在阿尔茨海默症(AD)的战场上,现有药物可谓“伤敌一千,自损八百”。
——虽能延缓病情进展,却要付出淀粉样蛋白相关影像学异常(ARIA)的代价,甚至有研究分析,抗淀粉样蛋白药物会将全脑萎缩速度推高21.8%。
寻找更为有效且安全的疗法是AD领域的当务之急。近日,国际期刊《Nature Medicine》(影响因子:58.7)公开了同种异体间充质干细胞(MSC)疗法——Laromestrocel(Lomecel-B)的最新实验数据。

△使用laromestrocel治疗轻度阿尔茨海默病的同种异体间充质干细胞疗法:一项随机对照2a期试验
该疗法此前就被FDA授予再生医学先进疗法(RMAT)认定,用于治疗轻度AD。而此次涉及49名患者的2a期实验结果更是让医疗圈振奋,它指向:
使用laromestroce可让轻度AD患者全脑萎缩速度减缓48.4%,海马体萎缩减少53%-62%,并减轻脑内炎症、改善患者认知功能。
而无论接受单次还是多次治疗,患者均未出现ARIA、超敏反应与严重不良反应,进一步证实了MSC在治疗AD上的安全性,有望成为AD治疗的新疗法。
01
全脑萎缩速度减半
干细胞2a期试验结果喜人
一旦患上AD,就像是走上了一条“脑部退行”的不归路,患者会逐渐出现记忆障碍、失语、失用、失认、视空间技能损害、执行功能障碍。在很长一段时间,人们都无法明确它的发病机制,而随着各类假说涌现,研究者也意识到炎症状态是痴呆表现的主要因素。
据观察:促炎因子会在淀粉样蛋白沉积物和神经原纤维缠结附近集结,全身炎症与Aβ积累之间存在关联等。
而过往研究证明:MSC能从细胞层面提供完整的沟通机制,通过异细胞偶联,细胞因子、生长因子和其他生物活性分子的释放发挥抗炎、促血管再生的特性,也因此被视作治疗AD的潜力方案。
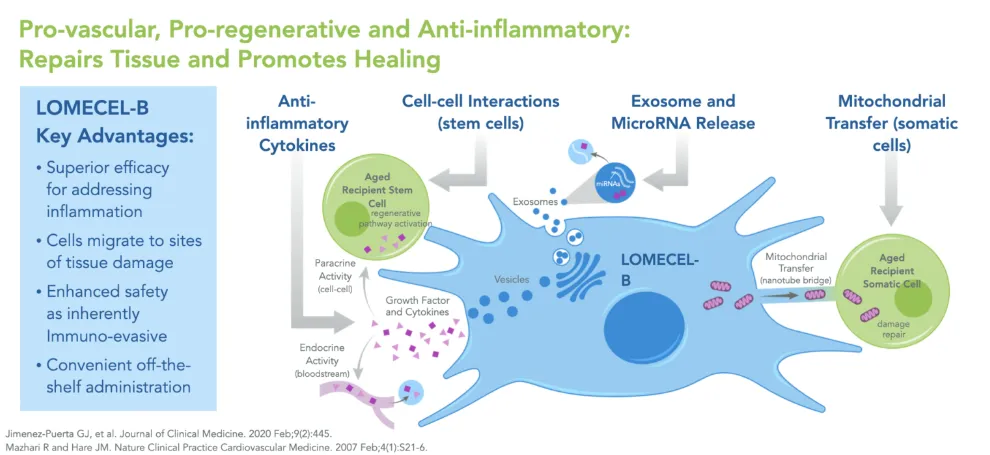
△间充质干细胞具有多效性作用机制(MOA)
美国Longeveron公司联合迈阿密大学的研究者们致力于该方向的研究,他们在2021年发布了骨髓来源的间充质干细胞药品Lomecel-B治疗阿尔茨海默症的1期试验结果。共有33名研究者参与研究,结果显示:患者对MSC药品耐受性良好,生活质量及神经认知提升,且多项抗炎血清生物标志物显著高于安慰剂组,提示MSC有改善炎症的潜力。
1期实验优秀的结果敦促着研究者迈入下一个阶段,此次2a期试验共招募49名轻度阿尔茨海默症患者参与,并按照1:1:1:1分为四组,治疗时间均为4个月。其中,组1为安慰剂组(每月一次安慰剂),组2第一剂输注2500万个MSC,后三个月每月接受一次安慰剂注射(低剂量组),组3每月输注一次2500万个MSC(中剂量组),组4每月输注一次1亿个MSC(高剂量组)。
主要探索终点为治疗后4周内严重不良事件(SAE)发生率。次要终点为39周时复合阿尔茨海默病评分(CADS)、认知功能(MoCA、MMSE)、日常生活能力(ADCS-ADL)及脑体积变化(MRI)。
结果显示:主要终点达成,各组SAE发生概率无明显差异,无输注反应、过敏或ARIA事件。
次要结局方面,安慰剂组CADS呈进行性下降,反映患者疾病持续恶化,对比来看,治疗组2-4在第39周评估时有临床改善。
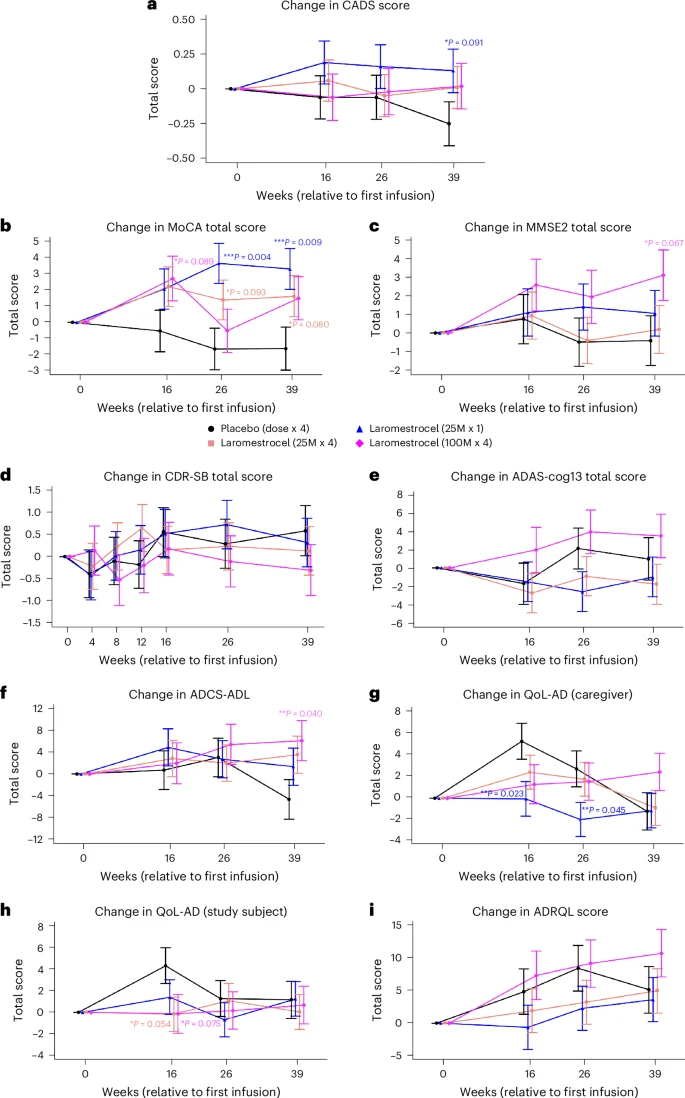
△次要结局一览
与出现全脑和多个脑区体积持续萎缩的安慰剂组相比,所有治疗组呈现了另一番景象——综合将全脑体积下降速度减缓48.4%(其中组3表现最亮眼,减缓了约57%)。海马体区(通常在疾病早期就开始萎缩)萎缩减少53%-62%,且与MMSE评分变化相关。此外,脑室扩大、灰质萎缩和颞叶皮层萎缩等方面也表现出不同的改善趋势。
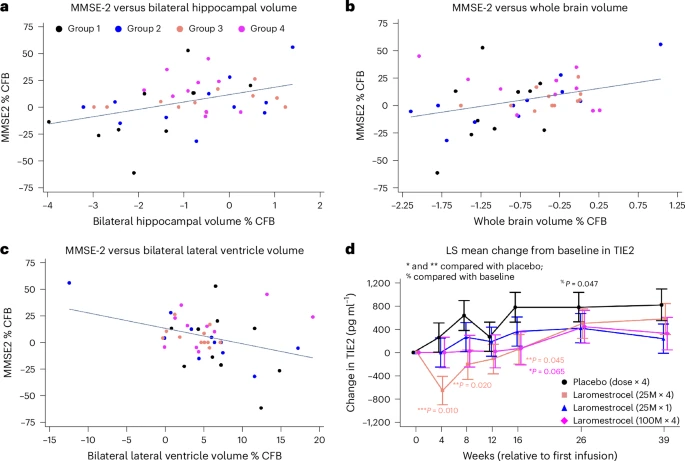
△双侧海马体、全脑萎缩的减少与MMSE评分的提高相关
一切研究结果显示:Laromestrocel能够减缓阿尔茨海默症患者脑萎缩和认知衰退,同样值得注意的是,相比于有ARIA风险的抗淀粉样蛋白药物,laromestrocel表达保护性神经血管和抗炎效应,有可能在联合治疗中帮助抵消ARIAs,呈现良好的安全性。
这些结果也支持Laromestrocel继续进行更大规模的3期试验,以进一步证实其有效性及安全性。
02
终结“漫长的告别”
干细胞展现AD治疗非凡前景
Laromestrocel的2a期试验向我们证明:拥有抗炎、促血管再生等特性的干细胞在治疗阿尔茨海默症上的卓越潜能,这并不是第一次,在此之前一众研究也在为此提供着证据。
2020年,《Advanced Science》(影响因子:14.3)上一则研究探索了临床级间充质干细胞的腹膜内给药对老年痴呆衰老加速小鼠的影响。

△HGF介导临床级人类脐带源间充质干细胞改善衰老加速的老年痴呆小鼠模型的功能恢复
结果显示脐带间充质干细胞(hUC-MSCs)具有修复损伤神经细胞的功能,能够通过HGF-cMet-AKT-GSK3β通路调节tau蛋白磷酸化,改善神经原纤维缠结,显著提高老年痴呆模型动物的学习记忆和认知能力。研究还提到:干细胞能促进老年小鼠大脑中的神经突触连接—这些都是阿尔茨海默症的关键特征。
加州大学圣地亚哥分校也得到了类似的结果,研究人员证明,干细胞可以有效挽救阿尔茨海默病小鼠模型中的多种体征和症状,与其他阿尔茨海默病小鼠相比,接受健康干细胞的小鼠表现出记忆和认知保留,神经炎症减少,β-淀粉样蛋白的积累显著减少。
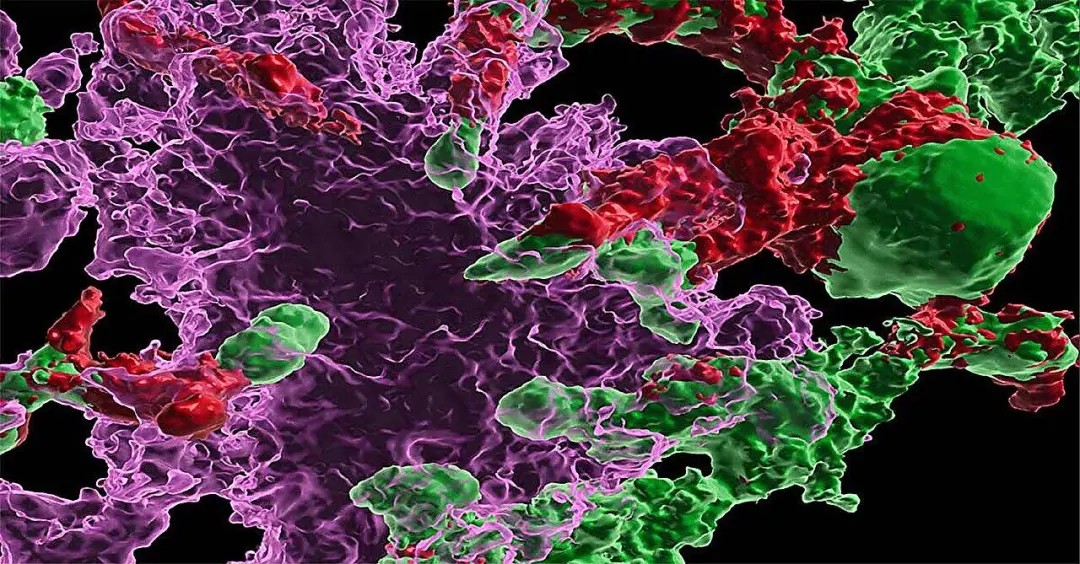
△野生型造血干细胞和祖细胞(绿色)的系统移植导致它们分化为小胶质细胞样细胞(红色),从而减少了大脑中β淀粉样斑块(洋红色)的数量
除了直接治疗,来自加州大学的研究者还想“借”干细胞的再生分化能力攻克阿尔茨海默症,他们瞄准神经系统疾病的关键驱动因素——小胶质细胞,结合当下大热的CRISPR基因编辑技术开发了一个前沿平台,通过筛选来自人类诱导多能干细胞(iPSCs)的小胶质细胞,系统性揭示小胶质细胞状态的调控因子,从而实现其功能表征和治疗靶向,为开发阿尔茨海默症的新疗法打开了新的大门。
总的来说,科学家正在干细胞这条再生道路上不断探索,或能为如今5800万阿尔茨海默症患者带去新的希望。