阿尔茨海默症(Alzheimer's Disease, AD),医学界曾长期称之为“老年痴呆症”,是一种以进行性认知功能丧失为特征的神经退行性疾病。它如同一种隐匿的“脑内侵蚀者”,从海马体和皮层开始,逐步瓦解患者的记忆储存、逻辑思维甚至基本生活能力。
在病程早期,患者可能遗忘近期对话或重复提问,随着神经元不可逆的损伤加剧,定向障碍、性格改变等症状相继出现。晚期患者将丧失语言能力、行动能力,甚至无法识别至亲的面容——这种从“自我”中逐渐剥离的过程,不仅让患者深陷混沌,更令家庭承受难以言喻的情感与经济重负。
随着全球人口老龄化不断加剧,阿尔茨海默病患者数量已接近5500万,并且预计到2050年这一数字将突破1亿。
面对如此庞大的患者群体,当前临床上有效的治疗方案依然十分匮乏。近年来,干细胞技术的迅速崛起为这一困境带来了新希望。干细胞不仅具有促进神经细胞再生和修复的潜力,还能通过调节免疫功能发挥神经保护作用。
越来越多的临床案例显示,干细胞干预在改善病理状态、延缓认知功能衰退方面具有明显优势,有望为阿尔茨海默病患者提供全新的治疗选择。
01
“脑海中的橡皮擦”:
阿尔兹海默症
阿尔茨海默症(Alzheimer’s disease,AD),常被人比喻为“脑海中的橡皮擦”,这是一种中枢神经系统的退行性病变,主要发生在老年或老年前期,其核心病理特征包括:
● β-淀粉样蛋白(Aβ)沉积:异常折叠的Aβ蛋白在脑内形成斑块,破坏神经元功能。
● Tau蛋白过度磷酸化:导致神经纤维缠结,阻碍细胞内物质运输。
● 神经炎症反应:小胶质细胞异常激活,释放炎性因子加速神经元死亡。
● 血管因素与遗传风险:载脂蛋白E(APOE)ε4基因显著增加患病风险,血管损伤可能协同加重病情。
目前学界认为,AD是多种机制共同作用的结果,而非单一因素致病(2021年《Nature Reviews Neuroscience》综述)。
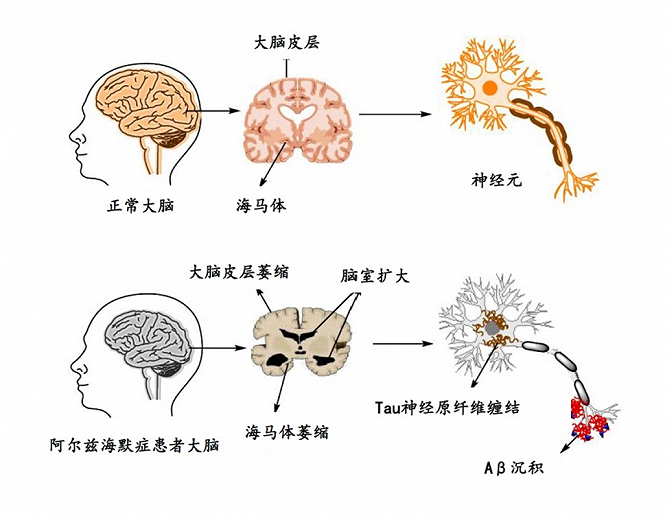
△ 正常大脑与阿尔兹海默症患者大脑和神经元生理结构
该病的主要特征包括进行性的认知功能障碍和行为损害。阿尔茨海默氏病是痴呆症最常见的形式,可能占病例数的60-70%。
中国是全球阿尔茨海默病患者最多的国家之一。2024年数据显示,中国60岁及以上人群中患者约1000万例,占全球病例的四分之一。预计到2050年,这一数字可能增长至3000万!(2023年《中国阿尔茨海默病报告》)仅15%-30%患者接受规范诊断,家庭年均照护成本达13万元,社会负担沉重。
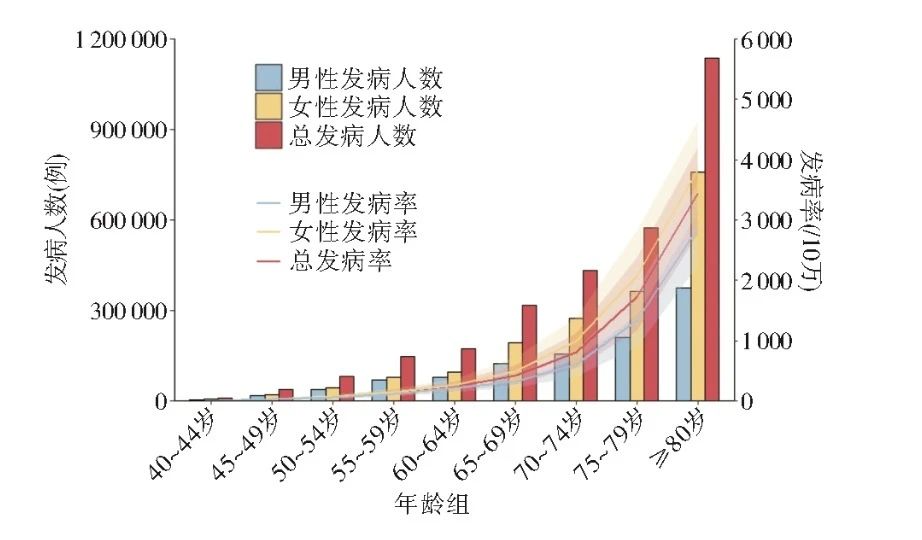
△ 图为2021年我国阿尔兹海默症及其他痴呆的分年龄组发病情况
目前,临床上的治疗方案主要是对症治疗和支持性管理。常用药物包括胆碱酯酶抑制剂(如多奈哌齐、利斯的明等),它们可以延缓神经递质分解,从而在一定程度上改善记忆和认知功能;另外,NMDA受体拮抗剂(如美金刚)也被用于调节神经兴奋性,减轻过度激活带来的神经损伤。
近年来,针对β-淀粉样蛋白沉积的单克隆抗体治疗和免疫疗法也逐渐进入临床试验阶段,虽然部分研究显示出一定疗效,但整体上这些新疗法尚未能显著改变疾病的进程。
此外,非药物治疗措施同样被广泛重视。例如,认知训练、物理锻炼和营养干预,以及家庭护理等,均对改善患者生活质量和延缓症状进展具有积极作用。
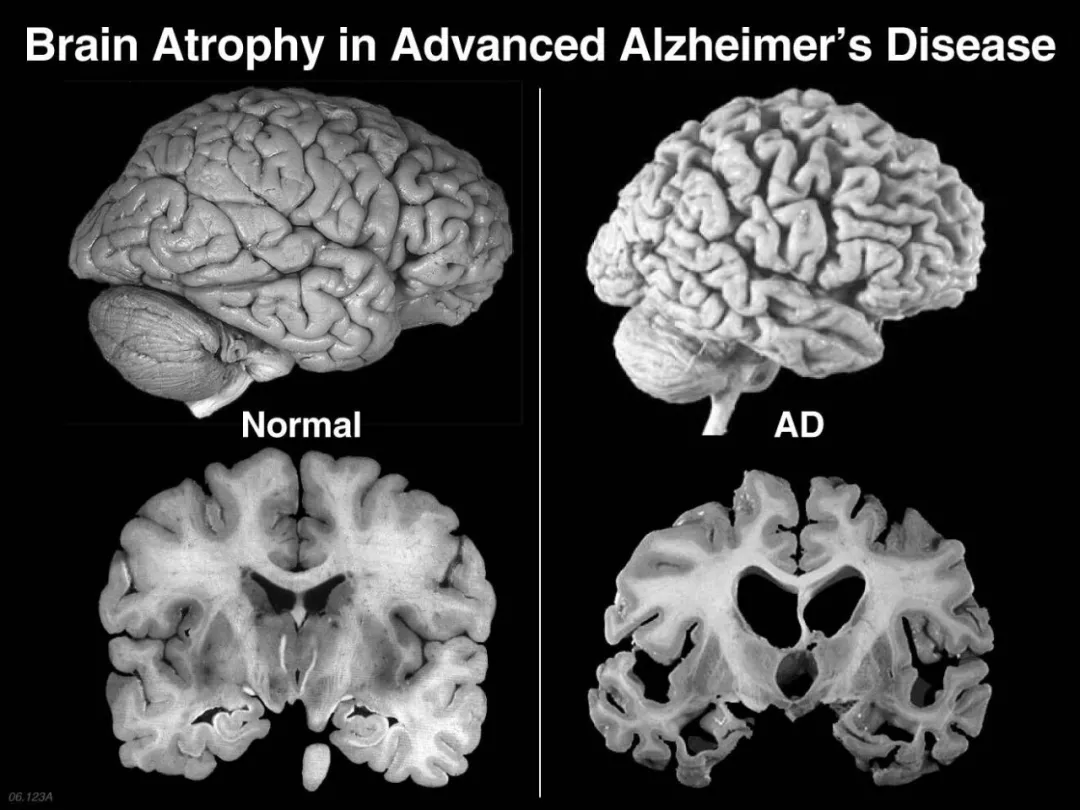
△ 大脑受损是阿尔兹海默病发生的原因
现有疗法仅能缓解症状,无法修复神经元或逆转病理进程。
02
干细胞疗法,
挽救“正在消失的记忆”
阿尔兹海默病虽然很难治愈,但作为退行性疾病,干细胞已经在该领域展现了不错疗效。
随着大脑衰老,大脑神经开始退化,尤其是神经元丧失和认知能力下降。有研究表明,阿尔兹海默病患者的神经和突触损失是该病症的两个标志性病变,也就是淀粉样蛋白β含斑块和神经原纤维缠结(NFTs的),这是由微管相关蛋白tau的高磷酸化形式。
而干细胞,尤其是间充质干细胞(hUC-MSC)保持较早的胚胎发育阶段,更年轻、产量更高,可以分泌多种功能因子,在多种疾病治疗中都展现了广阔的临床应用价值。
干细胞主要作用机制包括:
● 神经细胞再生:间充质干细胞(MSCs)可分化为神经元和胶质细胞,替代死亡细胞。
● 抗炎与免疫调节:干细胞分泌IL-10、TGF-β等因子,抑制小胶质细胞过度活化。
● 促进突触连接:干细胞释放BDNF(脑源性神经营养因子)、NGF(神经生长因子),修复神经网络。
● 清除异常蛋白:干细胞通过分泌Neprilysin等酶类,加速Aβ降解。
临床案例:
中国同济医学院(2021年):20例轻中度AD患者接受鼻内注射神经干细胞,6个月后MMSE评分平均提高3分(对照组下降1分)。
美国Longeveron公司(NCT04684602):Ⅰ期试验显示,骨髓MSCs治疗安全且耐受性良好,部分患者脑萎缩速率减缓。
随着再生医学技术的不断发展,越来越多的研究者正在探索通过干细胞移植、基因编辑等技术,来修复受损的神经元,恢复大脑认知功能。虽然这些研究目前仍处于临床试验阶段,但其潜力有目共睹,治疗效果也值得期待。
未来,干细胞再生医学将成为攻克阿尔兹海默病等神经性退行性疾病的新希望。