导语: 在癌症免疫治疗领域,CAR-T细胞疗法如同一颗耀眼的明星,为许多难治性血液肿瘤患者带来了希望。但您可能不知道,赋予T细胞这种“超能力”的核心部件——嵌合抗原受体,并非一成不变。它经历了一场持续数十年的精密“升级”,每一次迭代都旨在让这些改造后的免疫细胞变得更精准、更强大、更安全。今天,我们就来梳理一下CAR结构的演变历程,看看科学家们如何一步步优化这把对抗癌症的“分子钥匙”。
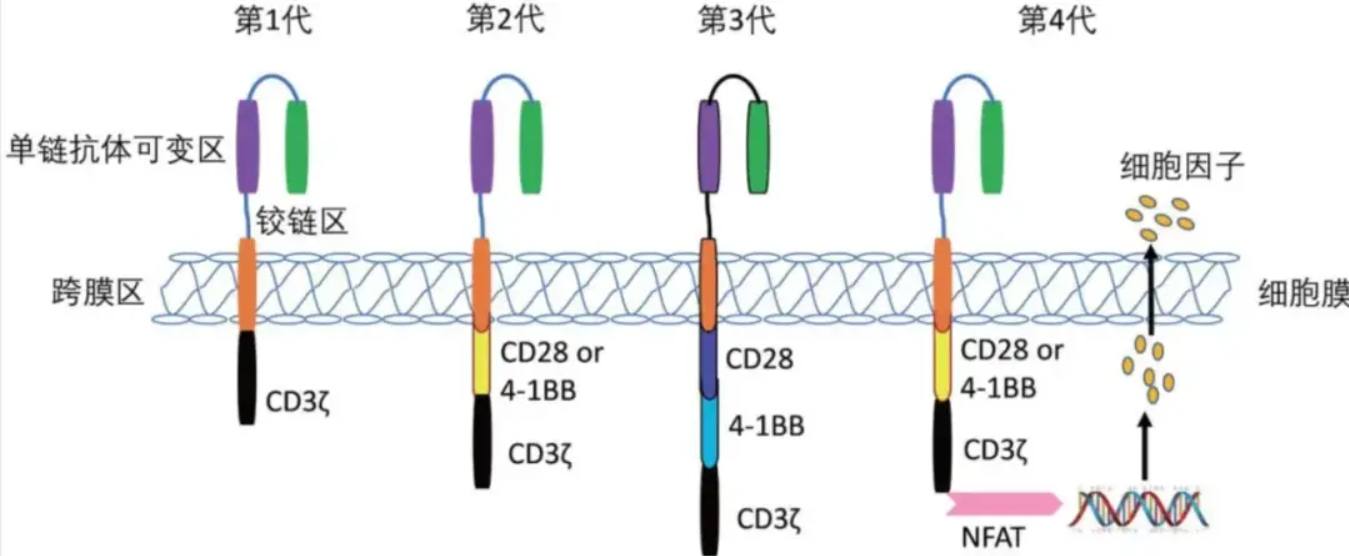
△ CAR-T历代结构演变示意图
01
初代CAR:识别的基础框架 (1989-2000)
胞外抗原结合域: 通常采用抗体的单链可变区片段,负责特异性识别肿瘤细胞表面的靶抗原(如B细胞肿瘤的CD19)。这是CAR的“眼睛”。
铰链/跨膜区: 连接胞外和胞内部分,提供结构灵活性。
胞内信号域: 仅包含T细胞受体复合物的核心激活信号元件——CD3ζ链。这是启动T细胞杀伤功能的基础开关。
成功实现了让T细胞绕过MHC限制,直接识别肿瘤抗原。能激活T细胞并诱导一定的杀伤活性。但激活信号单一且强度不足。改造后的T细胞在体内增殖能力弱、存活时间短,无法形成持续有效的抗肿瘤免疫应答,临床效果有限。
02
二代CAR:引入共刺激,实现质的飞跃 (2000至今主流)
在初代CD3ζ信号域的基础上,额外添加了一个共刺激信号域。这是CAR发展史上最关键的突破。
主要共刺激信号域:
CD28: 提供强烈的早期激活信号,促进T细胞快速扩增、细胞因子大量分泌(如IL-2),赋予强大的初始杀伤力。
4-1BB: 信号强度相对温和但持久,更侧重于促进T细胞的长期存活、记忆形成和线粒体生物合成,有助于维持持久的抗肿瘤活性,且与细胞因子风暴的相关性可能较低。
显著增强了T细胞的活化、增殖、存活和持续杀伤能力。基于CD19靶点的二代CAR-T疗法(如Kymriah, Yescarta)在复发/难治性B细胞白血病和淋巴瘤中取得了革命性的成功,并获得全球多国批准上市,成为当前临床应用的主流。但对实体瘤效果仍不理想,存在脱靶毒性、肿瘤微环境抑制等问题。
03
三代CAR:双重共刺激的探索
核心设计: 在CD3ζ基础上,同时整合两个不同的共刺激信号域(如CD28 + 4-1BB),意图获得更全面、更强的激活信号。
理论上结合了不同共刺激域的优势。但在实际临床前和临床研究中,相比成熟的二代CAR,其优势并未显著凸显。
结构更复杂,增加了潜在的不确定性和调控难度。
目前并非研发和临床应用的优先方向,更多作为探索性研究。
04
四代CAR/TRUCK:赋予“分泌”能力,改造微环境
在二代CAR结构的基础上,整合了可诱导表达的转基因元件。这些元件能在CAR识别肿瘤抗原后被激活。
分泌的功能分子:
增强CAR-T自身的存活、增殖和功能。募集和激活其他免疫细胞(如巨噬细胞、NK细胞、内源性T细胞),将“冷肿瘤”变“热”。
调节抑制性的肿瘤微环境。分泌细胞因子: 如IL-12, IL-15, IL-18, IL-7等。
设计更复杂,分泌因子的剂量、时机和安全性需要精细控制。
05
五代CAR:集成信号与智能逻辑控制
在二代基础上,进一步整合更下游的关键信号通路元件,并引入逻辑门控和安全开关设计。
关键组件:
自杀基因: 如诱导型Caspase9或单纯疱疹病毒胸苷激酶,可在发生严重副作用(如严重CRS或神经毒性)时,通过给予特定小分子药物,快速清除体内CAR-T细胞。
降解标签: 引入可被小分子诱导降解的蛋白标签,控制CAR蛋白本身的稳定性。
AND逻辑门: 要求T细胞同时识别两个不同的肿瘤抗原才完全激活,极大提高靶向特异性,减少对正常组织的脱靶毒性(尤其在靶抗原在正常组织也有低表达时)。
NOT逻辑门: 当存在特定健康组织标志物时,抑制CAR-T活性。
整合信号域: 除了CD3ζ和共刺激域,还可能包含直接激活其他关键通路(如JAK/STAT, PI3K)的域,意图获得更完整、更强的胞内信号传导。
实现更安全、更精准、更可控的CAR-T治疗,尤其为攻克实体瘤和拓展靶点提供可能。
06
CAR-T技术的进化远未停止
通用型CAR-T: 利用基因编辑技术(如CRISPR/Cas9)敲除供体T细胞的TCR和HLA分子,并可能进一步修饰降低宿主排斥反应,开发“现货供应”的异体CAR-T产品,降低成本,扩大可及性。
更精密的调控系统: 利用合成生物学设计更灵敏、可逆的基因开关(如光控、小分子控、表观遗传调控),实现CAR-T活性的动态、时空控制。
抵抗耗竭与微环境: 设计能抵抗T细胞耗竭、克服免疫抑制微环境(如TGF-β, 腺苷)的新型CAR结构或联合策略。
多功能集成平台: CAR-T细胞不仅是效应细胞,更可作为递送载体,分泌治疗性抗体、免疫调节剂或溶瘤病毒等,实现协同治疗。
写在最后
从简单的抗原识别器到集识别、激活、共刺激、微环境调节、逻辑门控和安全开关于一体的精密“活细胞药物”,CAR结构的演变是人类对免疫系统理解不断深入、基因工程技术飞速发展的直接体现。每一次结构升级,都围绕着提升疗效、降低毒副作用、拓展适应症的核心目标。虽然挑战犹存,尤其是在实体瘤领域,但持续优化的CAR设计,结合通用型平台、智能调控等前沿技术,正不断拓宽着CAR-T疗法的边界,为更多癌症患者带来新的希望。